Стволовые клетки в урологии
Каждая Нобелевская премия в области естественных наук – химии, физики и медицины и физиологии – не просто награда за выдающиеся открытия и прорывы. Это еще и знаковое событие в мире соответствующей науки, указывающее, как это принято говорить сейчас, на тренды.
|
|
Современная научная медицинская литература наполнена разрозненными сообщениями о стволовых клетках, генной инженерии, биотехнологиях и их применении в различных областях медицины. И если еще несколько десятков лет назад речь о применении стволовых клеток шла только теоретически, то сейчас технологии СК применяются практически, правда, только в рамках клинических исследований.Наше издание не осталось в стороне от мировых трендов – мы представляем новую рубрику «Инновации в урологии», где будут рассматриваться действительно принципиально новые технологии в урологии. Надеемся, что она станет постоянной и интересной для Вас, наши дорогие коллеги В этом отношении премия 2012 года в области физиологии и медицины (кстати, правильнее называть ее премией по физиологии ИЛИ медицине – именно так она именуется по-английски), врученная Джону Гердону и Синья Яманаке, может считаться классической. Ибо вручена она за работы в ключевой области современной науки – работы по клонированию и стволовым клеткам. Д. Гердон впервые смог клонировать лягушку из клеток эпителия, а С. Яманака сумел получить плюрипотентные стволовые клетки из обыкновенных дифференцированных клеток. Век назад такие вещи даже теоретически считались невозможными. |
|
Вспомнить все
Что же такое стволовые клетки (СК)? Это – источник обновления всех клеток организма, при этом из некоторых типов СК могут образовываться самые разные клетки. Из стволовых клеток растет эмбрион. Первая клетка, из которой получается наш организм – стволовая. Как и тысячи последующих клеток. Кстати, существование стволовых клеток предсказал великий русский гистологи эмбриолог Александр Александрович Максимов в 1908 году.
Существует несколько типов стволовых клеток. Самая универсальная стволовая клетка — зигота. Она дает началовсем типам клеток организма. Теми же свойствами обладают бластомеры —клетки, образовавшиеся при нескольких первых делениях зиготы. Из зиготы или бластомера можно вырастить целый организм. Такие клетки называются тотипотентными стволовыми клетками.
Чуть менее универсальны клетки, образующиеся при нескольких последующих зародышевых делениях (до разделения на зародышевые листки). Они могут дать начало всем клеткам организма, но не плаценте, поэтому целый новый организм из одной такой клетки вырастить невозможно. Эти клетки называются плюрипотентными стволовыми клетками (ПСК).
Уже специализированы мультипотентные стволовые клетки — то есть те, которые могут дать начало множеству клеточных типов, характерных для организма, но не всем. Мультипотентные клетки бывают, если можно так выразиться, «более или менее потентными» — то есть могут давать начало большему или меньшему количеству типов клеток.К мультипотентным относятся и некоторые из стволовых клеток, активных во взрослом организме, о которых говорилось выше. Постепенная дифференцировка потомков мультипотентных клеток приводит к появлению олигопотентных (дающих начало только небольшому количеству типов клеток) и унипотентных (дающих начало только одному типу) клеток.
Человеческий организм содержит примерно 50 миллиардов стволовых клеток, которые регулярно обновляются. С годами их количество сокращается, угасать они начинают уже к 20 годам, а в 70 лет их остается совсем немного. Для сравнения: у эмбриона — 1 стволовая клетка на 10тыс.обычных, у человека в 60-80 лет — 1 клетка на 5-8 миллионов.
Использование стволовых клеток в медицине началось достаточно давно и велось по двум направлениям: 1. инъекции соответствующих стволовых клеток в поврежденный орган и 2. попытки вырастить ткань или целый орган с последующей пересадкой его пациенту.
Второй путь хорош тем, что человек получает фактически новый здоровый орган вместо поврежденного или погибшего, при этом исключаются проблемы с совместимостью донорского органа. За последние годы ученые вырастили множество видов тканей и органов – от сердечного клапана до целого сердца. Правда, последнее еще не работает.
Не осталась в стороне и урология.
От мочевого пузыря из пробирки до почки из …принтера (!)
Урологическое сообщество в 2006 году взорвало сообщение группы Энтони Аталы из Северной Каролины. Оказывается, Э. Атала еще в 1999 году пересадил нескольким пациентам мочевой пузырь, выращенный с использованием стволовых клеток, но не опубликовал тогда результаты, дабы убедиться, что операция прошла успешно в отдаленном периоде времени. С тех пор в мире проведено около 30 подобных операций.
Сейчас Э. Атала – один из мировых лидеров нового направления в медицине, которое получило название тканевой инженерии. В его лабораториях ведутся работы над искусственным получением множества тканей и органов, не только урологических (несмотря на то, что Э. Атала – автор большой работы Stem Cell in Urology, опубликованной в 2008 году). Здесь выращивают хрящи,кости, сосуды, уретру и многие другие органы и ткани.
Пытаются здесь «работать» и над почками, которые вырастить гораздо сложнее, чем мочевой пузырь. Сам профессор Атала возлагает большие надежды на технологию 3D-печати, посредством которой орган можно будет просто напечатать из соответствующих клеточных культур. Впрочем, более простые случаи клеточной недостаточности пытаются лечить, делая инъекции стволовых клеток в начинающую давать сбои почку.
3D печать – это быстрое создание реальной модели по ее виртуальному образу. Технологический процесс 3D печати представляет собой послойное создание будущего предмета без использования форм или дополнительной оснастки. Существующие технологии позволяют создавать модели из пластика,гипса, специальных полимеров и прочих порошкообразных компонентов, которые могут склеиваться или спекаться в процессе создания прототипа.
Другие ученые пытаются работать «традиционным» методом: выращивать почку. Не так давно было опубликовано сообщение об успешно выращенных почечных канальцах почки человека.
А гарвардские специалисты во главе с Харальдом Оттом в апреле 2013 года сообщили, что им удалось вырастить целую почку крысы и пересадить ее живому грызуну. В этом случае в качестве «каркаса» использовалась почка умершей крысы, из которой удалили все клетки, кроме клеток соединительной ткани. Получившаяся почка содержала не все типы клеток, производила всего треть от нормального объема мочи и перерабатывала креатинин в 36 раз медленнее «естественной» почки. Но, тем не менее, это успех.
Тот же самый доктор Энтони Атала,впервые вырастивший и пересадивший мочевой пузырь человеку, в 2009 году провел еще один успешный эксперимент, правда, не на людях. Ему удалось вырастить и имплантировать ткань пещеристого тела полового члена. Не удивительно, что в качестве экспериментальных животных проф. Э. Атала с командой выбрали кроликов.
Эксперимент окончился удачно: 12 прооперированных кроликов спарили с самками, в результате четыре самки забеременели. Если технологию удастся перенести на людей, это будет важнейший прорыв в терапии выраженной эректильной дисфункции и серьезная альтернатива протезированию полового члена.
Интервью с профессором Энтони Атала, главой Института регенеративной медицины университета Wake Forest
Энтони Атала |
Конечно, никакие обзоры и статьи не могут заменить живого мнения ученого, который работает в этой области. Один из лидеров тканевой инженерии, первым в мире пересадивший человеку искусственно выращенный из стволовых клеток мочевой пузырь, тот самый доктор Энтони Атала, глава Института регенеративной медицины университета Wake Forest, любезно согласился дать блиц-интервью специально для «Дайджеста Урологии». После тяжелого операционного дня он нашел время, чтобы ответить на несколько вопросов, которые мы прислали ему по электронной почте. |
Каковы основные приоритеты в развитии технологий, связанных с использованием стволовых клеток в урологии?
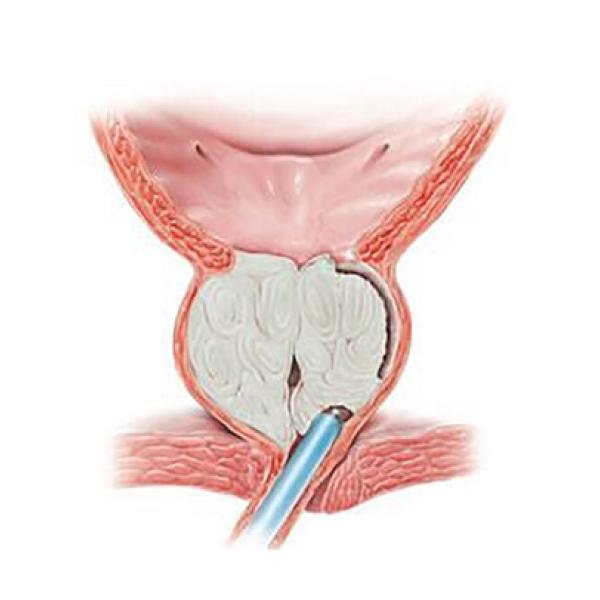
Стволовые клетки из мочевого пузыря (мышечные и эпителиальные) клинически используются для создания мочевого пузыря и уретры, которые имплантируются пациенту. Проекты, которые в настоящее время проходят предварительные клинические испытания, включают в себя использование мышечных клеток предшественников для лечения недержания мочи и клеток эректильной ткани для ее замещения.
Кроме того, ученые из Института регенеративной медицины Wake Forest проводят клинические исследования по применению трансплантации стволовых клеток сперматогенного эпителия в качестве потенциального лечения мужского бесплодия.
Когда впервые был создан искусственный орган мочевой системы? Когда он был впервые пересажен человеку? И какова судьба этого пациента?
Биоинженерный мочевой пузырь впервые был имплантирован пациенту в 1999 году. Мы докладывали об отдаленных результатах у семи пациентов в 2006 году. Обследование показало, что биоинженерные органы функционируют так же, как и органы, восстановленные с помощью кишечника, но без единого побочного эффекта. Эти пациенты чувствуют себя хорошо до сих пор.
Вы с тех пор выполняли подобные операции? Сколько из них находится по всему миру? Может ли Вы говорить о внедрении этого опыта в массовую практику?
После нашей пионерской работы мы лицензировали технологию для компании, которая продолжает проводить клинические испытания. Наша технология еще не прошла процедуру одобрения FDA, поэтому она недоступна вне рамок клинических исследований.
Каковы этапы формирования нового органа, например, мочевого пузыря? Сколько времени это занимает?
На создание мочевого пузыря в лаборатории уходит около 6-7 недель. Это период времени начинается небольшой биопсией c забором клеточного материала, продолжается выращиванием клеток и завершается имплантацией нового органа в тело пациента.
Есть ли какие-то отличия в случае создании почки? Трудно ли сделать почку? Сколько времени это займет?
Почка - намного более сложный орган, чем мочевой пузырь, и по количеству типов клеток (около 20), и по плотности. Мы изучаем несколько способов лечения почечной недостаточности - от использования 3D-печати для создания органа до инъекции стволовых клеток в орган. Основные проблемы с тканевой инженерией – это обеспечение адекватного снабжения клеток кислородом после имплантации.
Нобелевская премия по медицине в 2012 году была вручена Шинье Яманака, который получал стволовые клетки из обычных соматических. У Вас нет планов повторить Ваш опыт с мочевым пузырем, но применения соматических клеток в качестве первичного материала?
С нашей технологией тканевой инженерии идеальным будет использование собственных стволовых клеток пациента, так как не будет проблем с отторжением. Когда это невозможно, выходом является использование стволовых клеток из другого источника.
Какие глобальные достижения в этой области за последние 5 лет Вы находите наиболее важными?
Очень важными является развитие биопечати, а также, конечно, работы доктора Яманака и других ученых в области индуцированных плюрипотентных стволовых клеток.